摘要:USP <787>是针对治疗性蛋白质注射剂和相关制剂中颗粒物质而制定的法规,用以检查和记录制剂中亚可见颗粒物质的大小与数量。法规优先推荐使用光阻法。在检查治疗性蛋白注射制剂中亚可见颗粒的大小和数量时,USP<787>规定了对仪器、环境与背景、样品准备与测试样品的要求。本文将会对USP <787>进行解读,并用奥法美嘉公司的光阻法仪器AccuSizer A2000系列,按照USP <787>的要求对样品中亚可见颗粒大小和数量进行测试,来评判样品是否符合药典要求。
关键字:治疗性蛋白质注射剂、颗粒物质、光阻法、AccuSizer A2000系列
一、前言
治疗性蛋白注射剂一部分是由生物技术制造的蛋白质或多肽制备而成,一部分是由天然来源的治疗性蛋白质制备而成。治疗性蛋白注射剂中的颗粒物质由来自各种来源的可移动的不溶解物质组成。这些颗粒可能是外来的,例如纤维素;或内在的,例如制造过程中添加的润滑剂;或固有的,如蛋白质颗粒等。为保证制剂在人体中使用的安全,要求制剂的颗粒物质在一定的限度内。检查治疗性蛋白注射制剂中亚可见颗粒的大小和数量时,USP<787>规定了对仪器、环境与背景、样品准备与测试样品的要求。
对于治疗性蛋白注射液中亚可见颗粒的测定,光阻法颗粒计数试验是最常用的方法。奥法美嘉公司的光阻法仪器AccuSizer A2000系列符合美国药典USP <787>、<788>、<789>、<1788>和中国药典0903等一系列法规,在制药行业的微粒监控方面有着广泛应用。

图1.奥法美嘉公司的AccuSizer A2000系列
二、对测试仪器的要求
使用一种合适的仪器,该仪器应基于光阻原理,并允许自行规定测定颗粒大小和数量。所选传感器必须适合预期的颗粒尺寸范围和预期的颗粒计数。以下几个因素:如样品体积精度、样品流速、传感器分辨率、校准和粒子计数精度,对仪器的正确操作非常重要,它们在《USP 1788注射和眼科溶液中粒子物质的测定方法》里有详细规定,仪器必须要符合此规定。对于设备校准,要使用NIST可溯源粒度标准粒子或等效的可溯源标准粒子,这些标准粒子粒径一般在2到100微米之间。
仪器性能的验证要使用USP颗粒计数标粒,详情可参阅USP<1788>。
三、环境与背景要求
环境要求
所有操作最好在洁净台里进行。使用的玻璃器皿和设备应适当清洁和处理,以保持无颗粒。应尽量减少对制剂(液体或重组粉末)的震动和其他应力,并防止在检查时将气泡引入制剂。
背景要求
测定五份等分的脱气无颗粒水或合适的溶剂,10µm或10µm以上的颗粒数量超过1个颗粒/ mL,则检测背景不够干净。重复准备步骤,直到背景检测干净。
四、样品准备
如果每个样品单位体积足够大,就测试各个单元。如果体积太小,混合单元并组合内容物以获得所需的体积(通常为0.2~5.0mL)。取出样品,轻轻混合,测试四小份试样。
计算感兴趣尺寸范围内的颗粒,包括颗粒≥10μm和25µm的数目。舍掉第一个结果,然后取后三个结果的平均值。
此外,稀释是允许的,只要稀释剂和方法被证明是适当的。
五、对测试样品的要求
对于标称容积超过100毫升容器中提供的制剂,≥10μm的粒子数每毫升不超过25颗,≥25μm的粒子数每毫升不超过3颗。
对于标称容积少于和等于100毫升容器中提供的制剂,每个容器中≥10μm的粒子总数不超过6000个,≥ 25μm的粒子总数不超过600个。
六、AccuSizer A2000系列测试蛋白注射液样品
图2是测试一个蛋白注射液样品,其单个容器的标示容积大于100毫升,连续测试四个样品,测试结果如图:
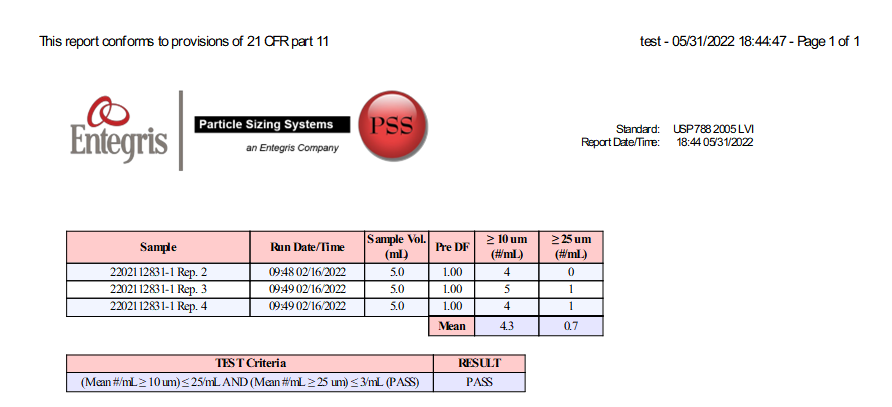
图2.某蛋白注射制剂样品的亚可观察颗粒物测试结果
舍弃第一个样品数据,取后三个样品平均值,样品的最终结果符合USP<787>中对蛋白注射制剂的要求,判断为合格。
USP <787>测试的许多准备和测量步骤与USP<788>相同。标准的AccuSizer A2000系统(图1)非常适合执行这些测试。另外一个重要的点是,USP <787>的可接受样品体积是0.2毫升(200µL),而A2000系列采样器可准确测量的样品体积远小于0.2毫升,使其非常适合于小体积蛋白质样品的分析。
七、结论
USP<787>是针对于治疗性蛋白质注射液中的亚可见颗粒物,而制定的法规。它对检测仪器、环境和背景、样品里的亚可见颗粒物数目大小和其它一些相关内容作出了规定,其内容严谨而详细。奥法美嘉公司的光阻法仪器AccuSizer A2000系列,符合USP <787>和其它一系列光阻法仪器法规,在制药行业中有着广泛应用。A2000系列的采样器可准确测量的样品体积远小于0.2毫升,使其非常适合于小体积蛋白质样品的分析。














