介绍:分散液(固体/液体)和乳剂(液体/液体)都是两相分散,溶剂为连续相,而颗粒或乳状液滴构成分散相。在稳定的分散体中,分散相的粒子大小随时间保持一致并保持悬浮状态。不稳定的乳状液会相分离,油相“奶油化”到溶液顶部,或者由于聚集或Ostwald成熟,乳状液滴会随着时间而增加。不稳定的悬浮液会絮凝/聚集,然后沉降到底部,如图1所示。
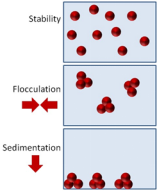
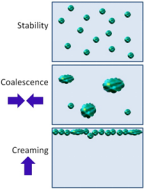
图1:稳定与不稳定
创建稳定的分散体需要控制连续相和分散相的化学和物理性质。通过选择表面活性剂,改变浓度、盐浓度、pH值,可以使连续相的化学性质得到优化。通过在表面(固态稳定)上添加聚合物涂层或/和增加表面电荷(静电稳定),可以使分散的相位更加稳定。当粒子表面没有电荷时,粒子相互紧密地接近,容易聚集,进而降低分散系的稳定性。但如果粒子表面电荷足够,粒子会像磁铁一样相互排斥,且不聚合,如图2所示。
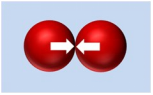
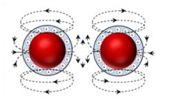
图2:吸引粒子聚集(左),排斥粒子分离(右)
从测量的角度看,表面电荷是用Zeta电位分析表征的。如图3所示,Zeta电位是距离粒子较短距离内的电位,单位为mV。在悬浮液上施加电场并通过电泳光散射检测粒子的运动来测量。粒子运动的方向决定了电性(+或-),而速度决定了电荷的大小。运动可以通过检测频移(相位多普勒)或相移(相位分析光散射或PALS)来分析。
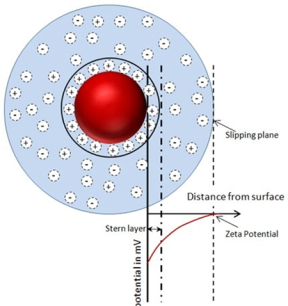
图3:Zeta电位
Zeta电位测量的主要结果是电泳迁移率µ,然后使用以下方程式计算Zeta电位:ζ=ƞμ/ɛ,在这里,ζ=Zeta电位,η=溶剂粘度,μ=电泳迁移率,ɛ=溶剂介电常数。zeta电位的正负电荷不重要,重要的是绝对值大小,较高的Zeta电位绝对值表明分散的稳定性得到了改善。不同种类的分散体需要不同的电荷值以增强稳定性,如图4所示(仅粗略代表)。
|
样品类型 |
Zeta电位 |
|
仅金属 |
>40mV |
|
金属氧化物 |
>30mV |
|
聚合物 |
>20mV |
|
乳液 |
>10mV |
图4:Zeta电位稳定性指南
通过改变Zeta电位来增加稳定性通常仅对平均粒径小于1µm的小颗粒起重要作用,但乳液的粒径可能会更大。
等电点(IEP):分散体系中的等电点是指Zeta电位为0时的pH值。这是进行Zeta电位测量的一个常见原因,因为IEP表明了可能导致分散不稳定的表面化学条件,如图5所示。
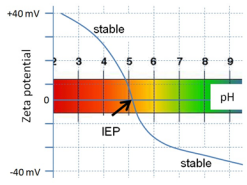
图5:等电点
结论:食品乳剂
通过用弱酸从pH6.8滴定到3.2来改变食品乳液的pH值。在每个pH值下,使用PALS技术(外加电场=4 v/cm)进行了七次测量,并报告了平均值。图6中显示了Zeta电位与pH的情况。
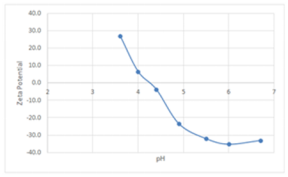
图6:Zeta电位与pH
图7显示了pH值为6.5时乳液样品的粒径分布,图8显示了pH值为3.5时乳液样品的粒径分布。注意,较低pH值时液滴粒径(302-496 nm)急剧增加时,表明乳液处于不稳定状态。
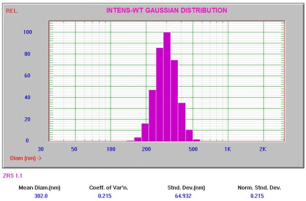
图7:pH值为6.5时的粒径,Zeta电位=-34 mV
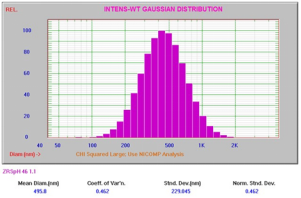
图8:pH值为4.6时的粒径,Zeta电位=-9.8 mV
结论:氧化锌悬浮液
购买了氧化锌(ZnO)“纳米粉末”(Sigma-Aldrich#544906),以研究pH值对zeta电位和粒径的影响。用Igepal CA-630非离子表面活性剂分散制备所有样品,并用超声波探头(2)超声3分钟。pH值为6.9和11.2的zeta电位值如图9和10所示。请注意,即使接近零,Zeta电位的结果也非常稳定。
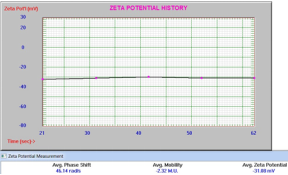
图9:ZnO在pH为6.9时的Zeta电位
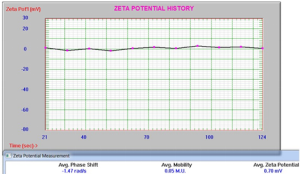
图10:ZnO在pH为11.2时的Zeta电位
图11显示了粒径的变化,从pH 6.9时198 nm处的单峰到pH 11.2时204和573 nm处的双峰分布。当zeta电位接近零时,悬浮液不稳定并开始聚集。
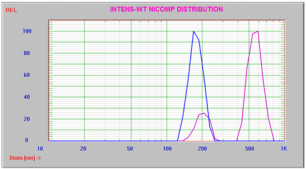
图11:ZnO在pH6.9(蓝)和11.2(粉)时的Zeta电位














